法规解读07丨Openlab Chemstation,现场审计都看些什么?
法规解读07丨Openlab Chemstation,现场审计都看些什么?
| 500 学员 |
| 学时: 5min |
| 课程数: 一节课 |
| 视频: 一个视频 |
| 色谱学堂 |
由于CFDA在《计算机化系统》这份文件中的语焉不详,
只要求进行计算机化验证,却没有明确验证的细节。
使得网络上产生了各式解读,
关于CSV计算机化验证要不要单独做,要怎么做,
争执的不可开交。

与此同时,
知名药企扬子江、康缘药业、正大天晴却早已先行一步,
纷纷做完CSV。
在8月份,
药明康德也刚刚完成了液相色谱网络版的全套计算机化验证。

他们是怎么做的呢?
是自己做还是请顾问公司来做呢?
重点和难点到底在哪里呢?
这一期,我们来聊聊CSV。

CFDA《计算机化系统》第十三条规定,
在计算机化系统使用之前,
应当对系统进行全面测试,
并确认系统可以获得预期的结果。

以往,法规只对仪器硬件确认有明确要求,
新的法规附录里要求进行基于风险评估的计算机化系统验证,
也就是对计算机、操作系统、应用软件和基础架构提出了新的验证要求。
只进行硬件的IQ/OQ/PQ是不够的,
还需要进行CSV 计算机化系统的验证
(CSV Computerized System Validation)。

在上一集中,我们提到软件升级实现合规的过程有点像房屋装修,
通过改造水电、防火设备来符合法规的要求。
对于会产生重大影响的房屋,
比如学校,医院,
在投入使用之前要请专业的机构来进行整体安全验收,
出具系统的文件,
这些文件将和其它的评估文件一起,
共同决定新的校区是否可以投入使用。
软件合规也是一样,
改造完毕之后,如何证明整套系统是合规的呢?
如何证明系统有着完善的审计追踪功能呢?
这就需要进行验证。

计算机化验证跟其它硬件的验证过程一样,
一方面需要设计验证的内容,
另一方面要整理验证的文件。
目的是通过纸质化的文件来证明计算机化系统符合法规的要求。

最主要的文件包括验证计划VP(Validation Plan),
用户需求规范URS(User Requirement Specification),
系统的风险评估报告,供应商审计报告,
IQ/OQ/PQ报告,一系列的管理规程和操作规程,
最后还要出具一个总的验证报告。
通常是先写验证计划VP,相当于总纲。
然后根据本身的需求来写用户需求规范URS。
不同的实验室,由于网络架构的差别,验证计划也会不同。
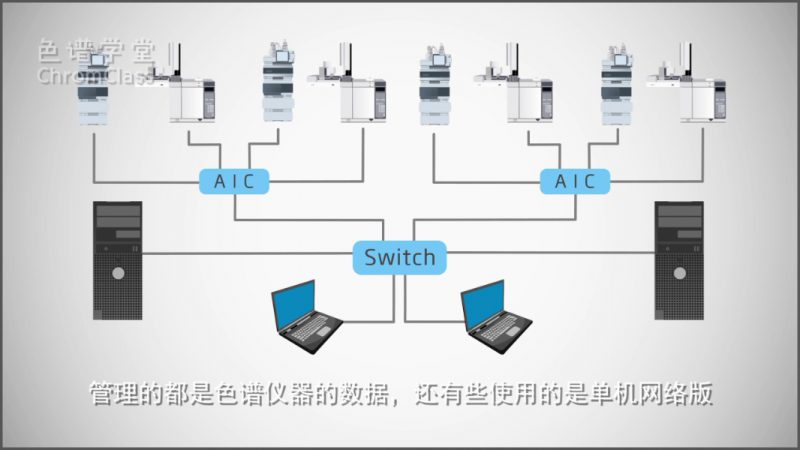
有些实验室是仪器厂商提供的网络版色谱软件,
管理的都是色谱仪器的数据。
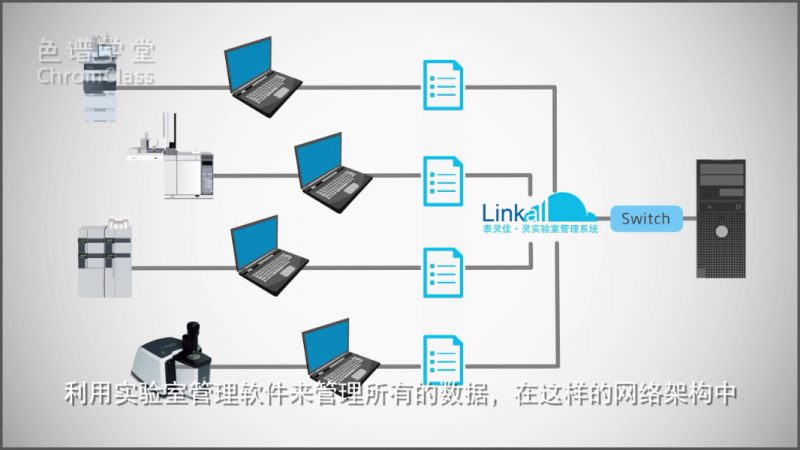
还有些使用的是单机网络版,
利用实验室管理软件,来管理所有的数据。
在这样的网络架构中,
除了色谱的数据,还包括紫外、红外这些光谱数据,
验证的内容就会更多一些。
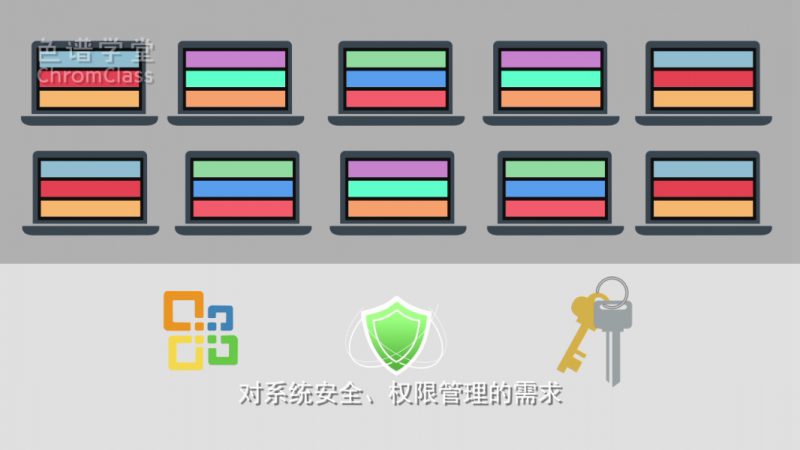
每台计算机的功能可能是有差别的,
用户需求规范URS应该单独写。
包括使用的功能性需求,对系统安全、权限管理的需求。
基于URS,要进行系统的风险评估。
根据软件的分类,还需进行对应的供应商审计。

色谱系统属于商业化程度比较高的系统,
一般进行邮政审计就好。
接下来是最为复杂的IQ/OQ/PQ的验证。
具体要验证哪些内容呢?
以审计追踪为例,验证内容包括:

1. 审计跟踪的信息是不是完整,
是否记录了修改时间,修改人,修改内容
2. 审计跟踪的记录是不是方便可查找,可导出

3. 数据变更的时候是不是都有记录变更理由
4. 验证审计跟踪的安全性,是不是不可删除,不可修改
5. 审计的动作是不是一旦开启,就不能关闭,是不是自动运行
6. 审计跟踪和原始记录的关联性是不是紧密
总之,与数据完整性有关的内容,是计算机化验证的重点。
也只有通过完整的CSV验证,
才能用文件的形式证明系统的合规。

要做好计算机系统验证,
首先要对于计算机系统熟悉和理解,了解网络架构,
还要理解法规要求,熟悉软件的结构和操作。
如果同学们还有什么疑问,欢迎给我们留言!

版权声明:本文版权属于色谱学堂(chromclass.com)所有,未经允许,禁止转载和摘编。如有需要,请联系market@chromclass.com 。
关于教员
购买过此产品并已登录的顾客才可发表评论。


目前还没有评论